报出死亡事件,美敦力召回栓塞装置
3152025-03-20 15:35:53
由于与该装置相关的多起死亡事件,美国食品药品监督管理局(FDA)将美敦力(Medtronic)对部分Pipeline VanTAGe栓塞装置的召回定性为“严重”。
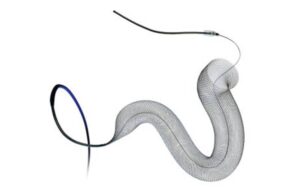
此次召回涉及停止使用和销售Pipeline VantaGE 027装置型号,并更新Pipeline VantaGe 021型号的使用说明。美敦力的Pipeline Vantage栓塞装置配备Shield Technology,用于治疗大脑动脉壁的膨出(动脉瘤)。这些血管内装置通过小导管进入血管,到达动脉瘤位置。在那里,一个小的编织管阻断流向膨出区域的血流。
根据FDA的通知,由于有报告称该装置的柔性编织管部分在使用过程中及使用后未能附着或保持附着在血管壁上(壁贴合不全和/或编织变形)的比率较高,美敦力召回并更新了装置的使用说明。
壁贴合不全和编织变形(也称为鱼口现象)、编织变窄或编织塌陷可能会发生。这些风险在女性中更高,尤其是年龄在45岁以下的女性。美敦力表示,使用受影响的产品可能会导致严重的健康后果,包括血栓形成、中风或死亡。
美敦力报告称,与Pipeline Vantage 027装置相关的伤害有13起,死亡4起。而对于Pipeline Vantage 021装置,报告的伤害有4起,没有死亡事件。
2025年1月30日,美敦力发出紧急医疗器械召回信,建议客户不要使用并退回所有未使用的027装置。在使用021装置之前,他们应阅读更新后的使用说明。更新使用说明旨在帮助实现最佳尺寸选择和支架编织部署。
对于已经使用受影响装置治疗的患者,治疗医生应根据患者的整体健康状况,决定是否需要进行后续影像学检查或改变医疗管理方案。这包括权衡双重抗血小板治疗的风险与编织变形的潜在风险。

