Medline紧急召回造影注射器及套装
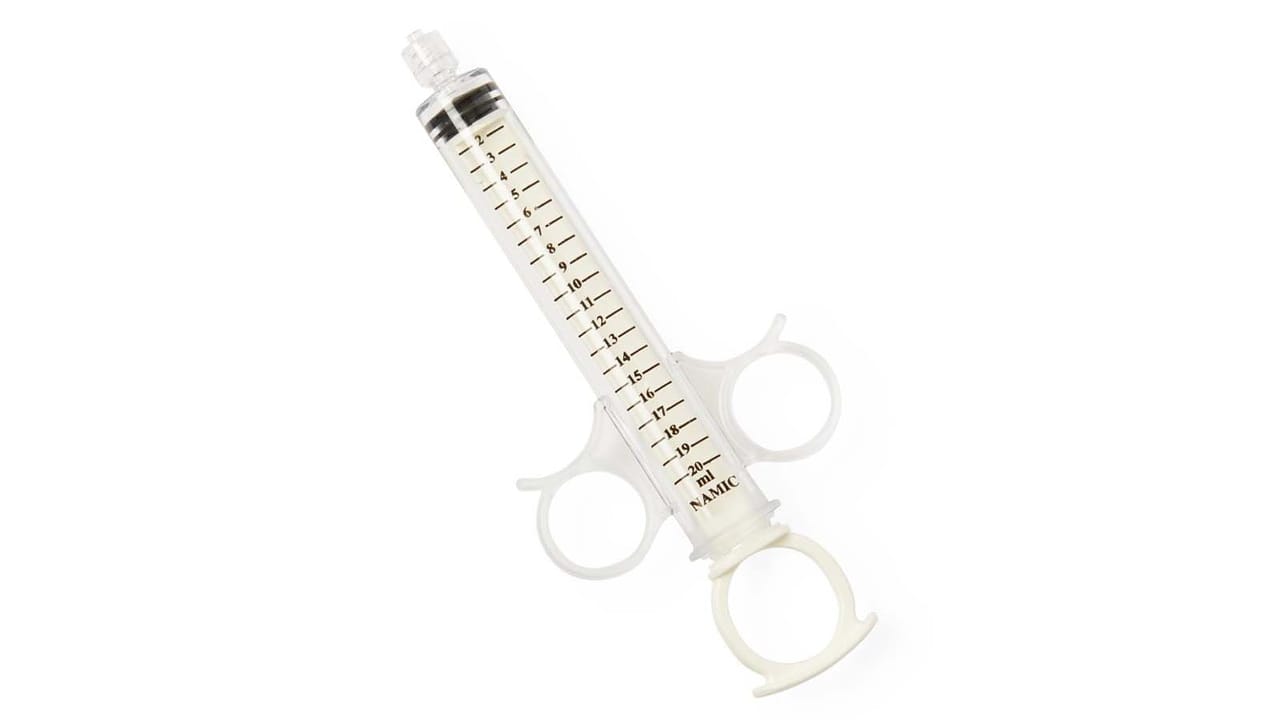
受影响设备上的注射器旋转适配器在使用过程中可能会松开,导致注射器与歧管之间的连接松动或完全断开。
FDA在2026年4月9日发布的一份声明中表示,Medline InDustries已对其Namic血管造影旋转适配器(RA)控制注射器及包含RA注射器的便利套装发布紧急医疗器械召回。
FDA表示,必须从使用或销售地点移除并销毁这些设备。该机构补充说,必须在手头所有受影响套装上贴上标签,说明受影响的注射器必须移除并丢弃,不得继续使用。
注射器可能与歧管断开
在召回通知中,Medline Industries表示,受影响设备上的注射器旋转适配器在使用过程中可能会松开,导致注射器与歧管之间的连接松动或完全断开。如果发生松开,可能存在生物危害暴露、失血和感染的风险。连接松动或断开可能会将空气引入管路,导致空气栓塞。这些情况可能导致严重伤害或死亡。所有单元都有可能表现出这种故障模式。
已收到221起投诉
截至2026年3月13日,Medline Industries已报告了四起与此问题相关的严重伤害事件,无死亡案例。FDA在3月25日发给Medline的警告信中指出,已收到221起与该设备相关的投诉,并提交了177份医疗器械报告(MDRs),涉及NAMIC血管造影控制注射器与歧管的断开,影响了患者和临床医生。
在发给Medline的CMS #723866号警告信中,FDA指出,在2025年12月对其纽约州格伦斯福尔斯工厂进行检查后,发现了质量体系违规规定。信中还指出,未能建立和维护验证设备设计的程序。
"具体而言,贵公司在'聚碳酸酯女鲁尔接头ISO 80369-7设计验证方案'下进行的设计验证……以及产生的'聚碳酸酯女鲁尔接头ISO 80369-7设计验证报告'……未能证明贵公司流体管理产品线(如旋塞阀产品系列、歧管产品系列、一次性传感器产品系列、Y型适配器等)的聚碳酸酯女鲁尔接头组件符合该标准规定的尺寸和功能测试要求,这些产品为符合BS EN ISO 80369-7而对其螺纹和锥度尺寸进行了变更,"FDA写道。
FDA认为公司回应不充分
该机构认为Medline对这封信的回应不充分。"贵公司应立即采取行动解决本信中发现的任何违规行为。未能充分解决此事可能导致FDA在不另行通知的情况下启动监管行动。这些行动包括但不限于扣押、禁令和民事罚款,"FDA写道。
在回应媒体询问时,Medline发言人表示,公司"认真对待这些事宜,[正在]直接与FDA合作解决观察结果,并已启动行动在需要的地方加强我们的流程。"

