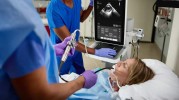
飞利浦推出用于重症监护的新型床旁超声系统
飞利浦推出了一款新型床旁超声系统(Flash 5100 POC),专为重症监护环境设计,配备人工智能驱动的自动化软件和大触摸屏,支持快速扫描并集成远程超声平台,助力临床医生在紧急情况下做出实时决策。...
Empatica的EpiMonitor获得MDR认证
Empatica的EpiMonitor癫痫监测解决方案在获得美国食品药品监督管理局(FDA)批准一年多后,现已获得MDR认证,并在欧洲上市。EpiMonitor是一种医疗级可穿戴设备和应用程序组合,旨...
智能手机可能提高医疗设备在不同肤色上的准确性
一项新研究表明,智能手机可以通过其摄像头客观测量肤色,从而提高医疗设备(如脉搏血氧仪)在不同肤色上的准确性,减少种族偏见。...
瑞凝生物Rembolic®肿瘤栓塞水凝胶入选“长三角区域重点领域医疗器械产品”
瑞凝生物的肿瘤栓塞水凝胶Rembolic®入选“长三角区域重点领域医疗器械产品”。该产品凭借其技术领先性和临床应用潜力,成功通过严格遴选和审评,有望推动中国精准介入治疗领域的发展。...
Inquis Medical的AVENTUS血栓切除系统获得FDA 510(k)许可,用于治疗肺栓塞
Inquis Medical的AVENTUS血栓切除系统获得FDA 510(k)许可,用于治疗肺栓塞。该系统结合了专有的组织感应技术,能够实时区分与导管尖端接触的组织类型,指导精确的血栓移除。...
英国医疗器械法规迎来重大改革
英国药品和健康产品管理局(MHRA)对医疗器械监管框架进行了重大改革,新的售后监管法规要求制造商积极跟踪已使用产品的安全性和性能,以更快地应对安全问题。...
OSSIO推出更小、更强、更智能的生物整合缝线锚钉,用于骨科手术
OSSIO公司推出了新一代生物整合缝线锚钉,用于骨科手术。这种2.5毫米的缝线锚钉比现有的生物复合材料锚钉具有更高的拉出强度,促进自然愈合,并且更容易与标准手术技术整合。...
HemoSonics的Quantra赢得2025年生命科学奖
HemoSonics的Quantra止血系统因其在粘弹性测试方面的工作赢得了2025年生命科学奖。该系统通过提供优化的凝血信息,加速手术室决策,改善患者结果,并降低医疗成本。...
Centerline因其涂层可能留在患者体内召回导丝
Centerline Biomedical公司因为其涂层可能在手术过程中脱落并留在患者体内,导致严重伤害或死亡的风险召回了用于血管手术的导丝。FDA已发布一级召回通知。...
Bracco Imaging和Subtle Medical获得AI驱动的MRI软件的CE认证
意大利的Bracco Imaging和Subtle Medical公司获得了欧盟CE认证,用于其共同开发的AI驱动的MRI软件AiMIFY,该软件能够增强对比MRI扫描的成像效果。...
- 热门文章
-
- 1北京天星医疗股份有限公司 - 中国最大国产运动医学植入物及器械提供商
- 2苏州赛纳思医疗技术有限公司(Sinus Medtech)
- 3波科国际医疗贸易(上海)有限公司
- 4重庆富沃思医疗器械有限公司(FWS Medical)
- 5湖南埃普特医疗器械有限公司(APT Medical)
- 6柯惠医疗器材国际贸易(上海)有限公司(Covidien Healthcare International Trading (Shanghai) Co., Ltd.)
- 7北京科仪邦恩医疗器械科技有限公司
- 8天津正天医疗器械有限公司(Tianjin Zhengtian Medical Devices Co., Ltd.)
- 9爱惜康有限责任公司 Ethicon, LLC - 全球外科缝合与微创医疗器械领导者
- 10北京瑞朗泰科医疗器械有限公司(Run-Long Medtech)
- 最近发表
-
- InVera Medical(英维拉医疗有限公司) - 爱尔兰慢性静脉疾病微创治疗先锋
- Invera Medical新型静脉输液设备获欧洲CE标志批准
- 1st SurgiConcept(第一外科概念) - 法国弹性提拉线(Spring Thread®)发明者
- (주)크리스탈옵틱(Crystal Optic Co., Ltd. / 韩国水晶光学有限公司) - 韩国医用放大镜专业制造商
- (주)워랜텍(Warantec Co., Ltd. / 韩国沃兰牙科器械有限公司) - 韩国牙科种植体先驱企业
- 10x Genomics, Inc.(10x Genomics股份有限公司) - 单细胞与空间生物学技术领导者
- 恩德威视株式会社(Endovision Co., Ltd. / (주)엔도비전) - 韩国创新型医疗器械与生物材料领军企业
- 3M Deutschland GmbH(3M德国有限公司) - 3M集团德国核心运营实体
- 3M Company(3M公司/明尼苏达矿业制造公司) - 全球科技创新与多元化制造巨头
- 3DHISTECH Kft.(3DHISTECH有限公司) - 欧洲数字病理学先驱与全球领导者
- 关注我们
-

扫一扫二维码关注我们的微信公众号